A. Sifat-Sifat Asam, Basa, dan Garam
Istilah asam (acid) berasal dari bahasa Latin acetum yang berarti cuka.
Seperti diketahui, zat utama dalam cuka adalah asam asetat. Basa
(alkali) berasal dari bahasa Arab yang berarti abu.
Seperti halnya dengan sabun, basa bersifat kaustik (licin), selain itu
basa juga bersifat alkali (bereaksi dengan protein di dalam kulit
sehingga sel-sel kulit akan mengalami pergantian). Rasa pahit merupakan
salah satu sifat zat yang bersifat basa.
Kita dapat mengenali asam dan basa dari rasanya. Namun, kita dilarang
mengenali asam dan basa dengan cara mencicipi karena cara tersebut bukan
merupakan cara yang aman. Untuk mengidentifikasi asam dan basa yang
baik dan aman dapat dengan menggunakan indikator. Indikator yaitu suatu
bahan yang dapat bereaksi dengan asam, basa, atau garam sehingga akan
menimbulkan perubahan warna.
1. Asam
Asam merupakan salah satu penyusun dari berbagai bahan makanan dan
minuman, misalnya cuka, keju, dan buah-buahan. Menurut Arrhenius, asam
adalah zat yang dalam air akan melepaskan ion H+. Jadi, pembawa sifat
asam adalah ion H+ (ion hidrogen), sehingga rumus kimia asam selalu
mengandung atom hidrogen. Ion adalah atom atau sekelompok atom yang
bermuatan listrik. Kation adalah ion yang bermuatan listrik positif.
Adapun anion adalah ion yang bermuatan listrik negatif.
Sifat khas lain dari asam adalah dapat bereaksi dengan berbagai bahan
seperti logam, marmer, dan keramik. Reaksi antara asam dengan logam
bersifat korosif. Contohnya, logam besi dapat bereaksi cepat dengan asam
klorida (HCl) membentuk Besi (II) klorida (FeCl2).
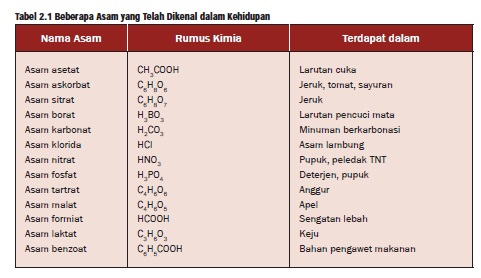
Tabel beberapa contoh asam
Berdasarkan asalnya, asam dikelompokkan dalam 2 golongan, yaitu asam organik dan asam anorganik. Asam organik umumnya bersifat asam lemah, korosif, dan banyak terdapat di alam. Asam anorganik umumnya
bersifat asam kuat dan korosif. Karena sifat-sifatnya itulah, maka
asam-asam anorganik banyak digunakan di berbagai kebutuhan manusia.
2.Basa
Dalam keadaan murni, basa umumnya berupa kristal padat dan bersifat
kaustik. Beberapa produk rumah tangga seperti deodoran, obat maag
(antacid) dan sabun serta deterjen mengandung basa.
Basa adalah suatu senyawa yang jika dilarutkan dalam air (larutan) dapat
melepaskan ion hidroksida (OH-). Oleh karena itu, semua rumus kimia
basa umumnya mengandung gugus OH.
Jika diketahui rumus kimia suatu basa, maka untuk memberi nama basa,
cukup dengan menyebut nama logam dan diikuti kata hidroksida.
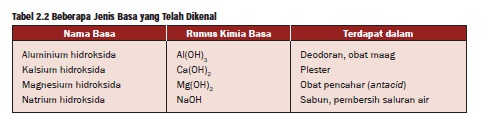
Tabel beberapa contoh Basa
Perbedaan Sifat Asam dan Basa
3. Garam
Orang mengalami sakit perut disebabkan asam lambung yang meningkat.
Untuk menetralkan asam lambung (HCl) digunakan antacid. Antacid
mengandung basa yang dapat menetralkan kelebihan asam lambung (HCl).
Umumnya zat-zat dengan sifat yang berlawanan, seperti asam dan basa
cenderung bereaksi membentuk zat baru. Bila larutan asam direaksikan
dengan larutan basa, maka ion H+ dari asam akan bereaksi dengan ion OH-
dari basa membentuk molekul air.
H+ (aq) + OH- (aq) —> H2O (ℓ)
Asam Basa Air
Karena air bersifat netral, maka reaksi asam dengan basa disebut reaksi penetralan.
Ion-ion ini akan bergabung membentuk senyawa ion yang disebut garam.
Bila garam yang terbentuk ini mudah larut dalam air, maka ion-ionnya
akan tetap ada di dalam larutan. Tetapi jika garam itu sukar larut dalam
air, maka ion-ionnya akan bergabung membentuk suatu endapan. Jadi,
reaksi asam dengan basa disebut juga reaksi penggaraman karena membentuk
senyawa garam.
Mari kita simak contoh reaksi pembentukan garam berikut!
Mari kita simak contoh reaksi pembentukan garam berikut!
Asam + Basa —> Garam + Air
Asam klorida + Natrium hidroksida —> Natrium klorida + air
HCl (aq) + Na OH (aq) —> Na Cl (aq) + H2O (ℓ)
Asam Basa Garam Air
Walaupun reaksi asam dengan basa disebut reaksi penetralan, tetapi hasil
reaksi (garam) tidak selalu bersifat netral. Sifat asam basa dari
larutan garam bergantung pada kekuatan asam dan basa penyusunnya.
Garam yang berasal dari asam kuat dan basa kuat bersifat netral, disebut
garam normal, contohnya NaCl dan KNO3. Garam yang berasal dari asam
kuat dan basa lemah bersifat asam dan disebut garam asam, contohnya
adalah NH4 Cl. Garam yang berasal dari asam lemah dan basa kuat bersifat
basa dan disebut garam basa, contohnya adalah CH3COONa.
Contoh asam kuat adalah HCl, HNO3, H2SO4. Adapun KOH, NaOH,
Ca(OH)2 termasuk basa kuat.
Contoh asam kuat adalah HCl, HNO3, H2SO4. Adapun KOH, NaOH,
Ca(OH)2 termasuk basa kuat.
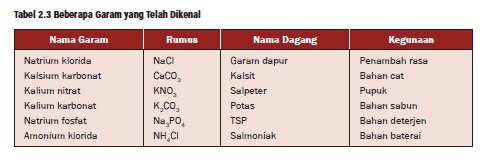
Tabel beberapa contoh garam
4. Larutan Asam, Basa, dan Garam Bersifat Elektrolit
Ketika seseorang mencari ikan dengan menggunakan ”setrum” atau aliran
listrik yang berasal dari aki, apa yang terjadi setelah beberapa saat
ujung alat yang telah dialiri arus listrik itu dicelupkan ke dalam air
sungai? Ternyata ikan yang berada di sekitar ujung alat itu terkena
aliran listrik dan pingsan atau mati.
Apakah air dapat menghantarkan listrik?
Sebenarnya air murni adalah penghantar listrik yang buruk. Akan tetapi
bila dilarutkan asam, basa, atau garam ke dalam air maka larutan ini
dapat menghantarkan arus listrik. Zat-zat yang larut dalam air dan dapat
membentuk suatu larutan yang menghantarkan arus listrik dinamakan
larutan elektrolit. Contohnya adalah larutan garam dapur dan larutan
asam klorida. Zat yang tidak menghantarkan arus listrik dinamakan
larutan nonelektrolit. Contohnya adalah larutan gula dan larutan urea.
Untuk mengetahui suatu larutan dapat menghantarkan arus listrik atau
tidak, dapat diuji dengan alat penguji elektrolit. Alat penguji
elektrolit sederhana terdiri dari dua elektroda yang dihubungkan dengan
sumber arus listrik searah dan dilengkapi dengan lampu, serta bejana
yang berisi larutan yang akan diuji. Mari kita lakukan kegiatan berikut
untuk mengetahui apakah asam, basa, dan garam dapat menghantarkan arus
listrik.
B. Identifikasi Asam, Basa, dan Garam
Banyak sekali larutan di sekitar kita, baik yang bersifat asam, basa,
maupun netral. Cara menentukan sifat asam dan basa larutan secara tepat
yaitu menggunakan indikator. Indikator yang dapat digunakan adalah
indikator asam basa. Indikator adalah zat-zat yang menunjukkan indikasi
berbeda dalam larutan asam, basa, dan garam. Cara menentukan senyawa
bersifat asam, basa, atau netral dapat menggunakan kertas lakmus dan
larutan indikator atau indikator alami.
Berikut adalah beberapa cara menguji sifat larutan.
1. Identifikasi dengan Kertas Lakmus
Warna kertas lakmus dalam larutan asam, larutan basa dan larutan
bersifat netral berbeda. Ada dua macam kertas lakmus, yaitu lakmus merah
dan lakmus biru. Sifat dari masing-masing kertas lakmus tersebut adalah
sebagai berikut.
a. Lakmus merah dalam larutan asam berwarna merah dan dalam larutan basa berwarna biru.
b. Lakmus biru dalam larutan asam berwarna merah dan dalam larutan basa berwarna biru.
c. Lakmus merah maupun biru dalam larutan netral tidak berubah warna.
b. Lakmus biru dalam larutan asam berwarna merah dan dalam larutan basa berwarna biru.
c. Lakmus merah maupun biru dalam larutan netral tidak berubah warna.
2. Identifikasi Larutan Asam dan Basa Menggunakan Indikator Alami
Cara lain untuk mengidentifikasi sifat asam atau basa suatu zat dapat
menggunakan indikator alami. Berbagai bunga yang berwarna atau tumbuhan,
seperti daun, mahkota bunga, kunyit, kulit manggis, dan kubis ungu
dapat digunakan sebagai indikator asam basa. Ekstrak atau sari dari
bahan-bahan ini dapat menunjukkan warna yang berbeda dalam larutan asam
basa.
Sebagai contoh, ambillah kulit manggis, tumbuklah sampai halus dan
campur dengan sedikit air. Warna kulit manggis adalah ungu (dalam
keadaan netral). Jika ekstrak kulit manggis dibagi dua dan masing-masing
diteteskan larutan asam dan basa, maka dalam larutan asam terjadi
perubahan warna dari ungu menjadi cokelat kemerahan. Larutan basa yang
diteteskan akan mengubah warna dari ungu menjadi biru kehitaman.
C. Penentuan Skala Keasaman dan Kebasaan
1. Kekuatan Asam dan Basa
Kekuatan suatu asam atau basa tergantung bagaimana senyawa tersebut
dapat diuraikan menjadi ion-ion dalam air. Peristiwa terurainya suatu
zat menjadi ion-ionnya dalam air disebut ionisasi. Asam atau basa yang
terionisasi secara sempurna dalam larutan merupakan asam kuat atau basa
kuat. Sebaliknya asam atau basa yang hanya terionisasi sebagian
merupakan asam lemah atau basa lemah.
Jika ingin mengetahui kekuatan asam dan basa maka dapat dilakukan
percobaan sederhana. Perhatikan nyala lampu saat mengadakan percobaan
uji larutan elektrolit. Bila nyala lampu redup berarti larutan tergolong
asam atau basa lemah, sebaliknya apabila nyala lampu terang berarti
larutan tersebut tergolong asam atau basa kuat.
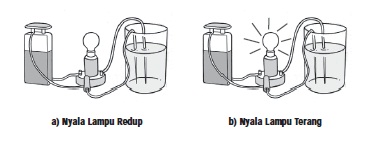
Asam kuat atau asam lemah pada konsentrasi yang sama menghantarkan
listrik yang berbeda. Nyala lampu pada Gambar (a) tampak redup. Ini
berarti larutan yang diuji berupa asam lemah atau basa lemah. Adapun
pada Gambar (b) lampu menyala terang, menandakan bahwa larutan yang
diuji berupa asam kuat atau basa kuat.
2. Derajat Keasaman dan Kebasaan (pH dan pOH)
Pada dasarnya derajat/tingkat keasaman suatu larutan (pH = potenz
Hydrogen)) bergantung pada konsentrasi ion H+ dalam larutan. Semakin
besar konsentrasi ion H+ semakin asam larutan tersebut.
Umumnya konsentrasi ion H+ pada larutan sangat kecil, maka untuk
menyederhanakan penulisan digunakan konsep pH untuk menyatakan
konsentrasi ion H+. Nilai pH sama dengan negatif logaritma konsentrasi
ion H+ dan secara matematika dinyatakan dengan persamaan
pH = – log (H+)
Analog dengan pH, konsentrasi ion OH– juga dapat dinyatakan dengan cara
yang sama, yaitu pOH (Potenz Hydroxide) dinyatakan dengan persamaan
berikut.
pOH = – log (OH-)
Derajat keasaman suatu zat (pH) ditunjukkan dengan skala 0—14.
a. Larutan dengan pH < 7 bersifat asam.
b. Larutan dengan pH = 7 bersifat netral.
c. Larutan dengan pH > 7 bersifat basa.
Jumlah harga pH dan pOH = 14. Misalnya, suatu larutan memiliki pOH = 5,
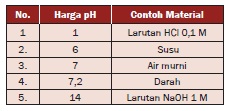
maka harga pH = 14 – 5 = 9. Harga pH untuk beberapa jenis zat yang dapat
kita temukan di lingkungan sehari-hari dinyatakan dalam Tabel.
Tabel Harga pH untuk Beberapa Jenis Zat
3. Menentukan pH Suatu Larutan
Derajat keasaman (pH) suatu larutan dapat ditentukan
menggunakan indikator universal, indikator stick, larutan indiaktor, dan
pH meter.
a. Indikator Universal.
Indikator universal merupakan campuran dari bermacam-macam indikator
yang dapat menunjukkan pH suatu larutan dari perubahan warnanya.
Indikator universal ada dua macam yaitu indikator yang berupa kertas dan
larutan.
b. Indikator Kertas (Indikator Stick)
Indikator kertas berupa kertas serap dan tiap kotak kemasan indikator
jenis ini dilengkapi dengan peta warna. Penggunaannya sangat sederhana,
sehelai indikator dicelupkan ke dalam larutan yang akan diukur pH-nya.
Kemudian dibandingkan dengan peta warna yang tersedia.
c. Larutan Indikator
Salah satu contoh indikator universal jenis larutan adalah
larutan metil jingga (Metil Orange = MO). Pada pH kurang dari 6
larutan ini berwarna jingga, sedangkan pada pH lebih dari 7 warnanya
menjadi kuning.
Contoh indikator cair lainnya adalah indikator fenolftalin
(Phenolphtalein = pp). pH di bawah 8, fenolftalin tidak berwarna, dan
akan berwarna merah anggur apabila pH larutan di atas 10.
d. pH Meter
Pengujian sifat larutan asam basa dapat juga menggunakan pH meter.
Penggunaan alat ini dengan cara dicelupkan pada larutan yang akan diuji,
pada pH meter akan muncul angka skala yang menunjukkan pH larutan.









Komentar
Posting Komentar